Overgangsalder innebærer en rekke fysiologiske forandringer ettersom kroppens hormonbalanse endres. Rundt 1 av 3 kvinner får betydelige symptomer, 1 av 3 får lite symptomer og 1 av 3 har noe plager. Hetetokter, humørsvingninger, urinveisproblemer og økt trang, søvnproblemer, nedsatt sexlyst, tørre slimhinner og andre vulvovaginale symptomer er vanlige*.
Vulvovaginal atrofi (VVA), som omfatter symptomer som kløe, svie og brennende følelse i underlivet samt smerter under samleie (dyspareuni), er en del av det som kalles urogenitalt syndrom som oppstår ved overgangsalder (menopause). Symptomene rammer omtrent 50 % av alle postmenopausale kvinner, og hvis dette ikke behandles forverres det ofte med årene på grunn av synkende nivåer av kjønnshormoner, noe som kan ha en betydelig negativ innvirkning på livskvaliteten2.
Eksempler på vulvovaginale symptomer:
Smerter ved samleie (dyspareuni) er et vanlig symptom ved vulvovaginal atrofi. I effektstudiene for Intrarosas var smerter ved samleie det symptomet som ble oppgitt som mest plagsomt1.
*Referanse: Helsenorge: Symptomer på overgangsalder (https://www.helsenorge.no/kvinnehelse/overgangsalder/symptomer/) 2026-02-27
Intrarosa er vagitorier beregnet for behandling av vulvovaginal atrofi (VVA) hos postmenopausale kvinner med moderate til kraftige symptomer.
Virkestoffet i Intrarosa er prasteron, dvs. dehydroepiandrosteron (DHEA), som er biokjemisk og biologisk identisk med endogent humant DHEA. DHEA er et inaktivt forløperhormon (prekursorsteroid) som omdannes til østrogener og androgener i perifert vev, som for eksempel vagina. Intrarosa er dermed forskjellig fra lokale østrogenpreparater ved at det også gir opphav til androgene metabolitter1.
DHEA dannes hovedsakelig i binyrene og er den eneste signifikante kilden til østrogener og androgener etter overgangsalder (menopausen)3,4.
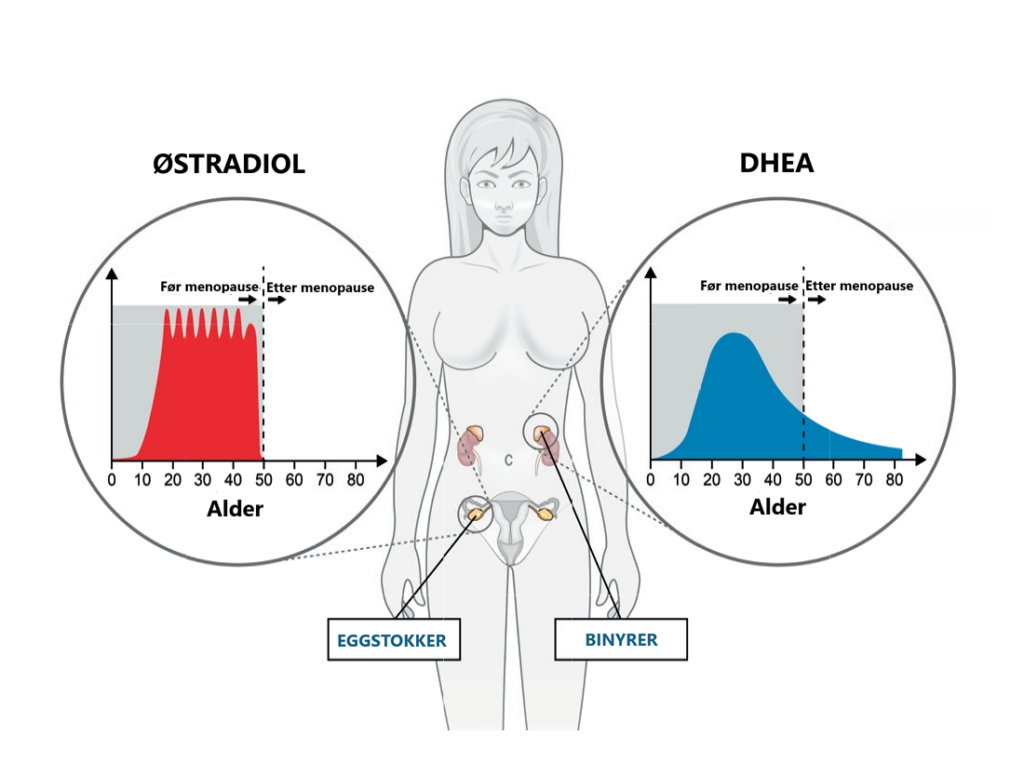
Skjematisk illustrasjon av nivåene av østradiol og DHEA før og etter overgangsalder (menopause).
Illustrasjon er tilpasset fra
Orentreich N et al. J. Clin. End. Met. 59, 551-555, 1984, Labrie F et al. J. Clin. Endocrinol. Met. 82, 2396-2402, 1997, Labrie F et al. Menopause. 18, 30-43, 2011, Labrie et al. Climacteric. 16, 205-213, 2013
Intrarosa administreres som en liten (lengde 28 mm) vagitorie. DHEA tas opp i vaginale celler og omdannes intracellulært til androgener og østrogener. De positive effektene på tegn og symptomer på vulvovaginal atrofi skyldes aktivering av vaginale østrogen- og androgenreseptorer1.
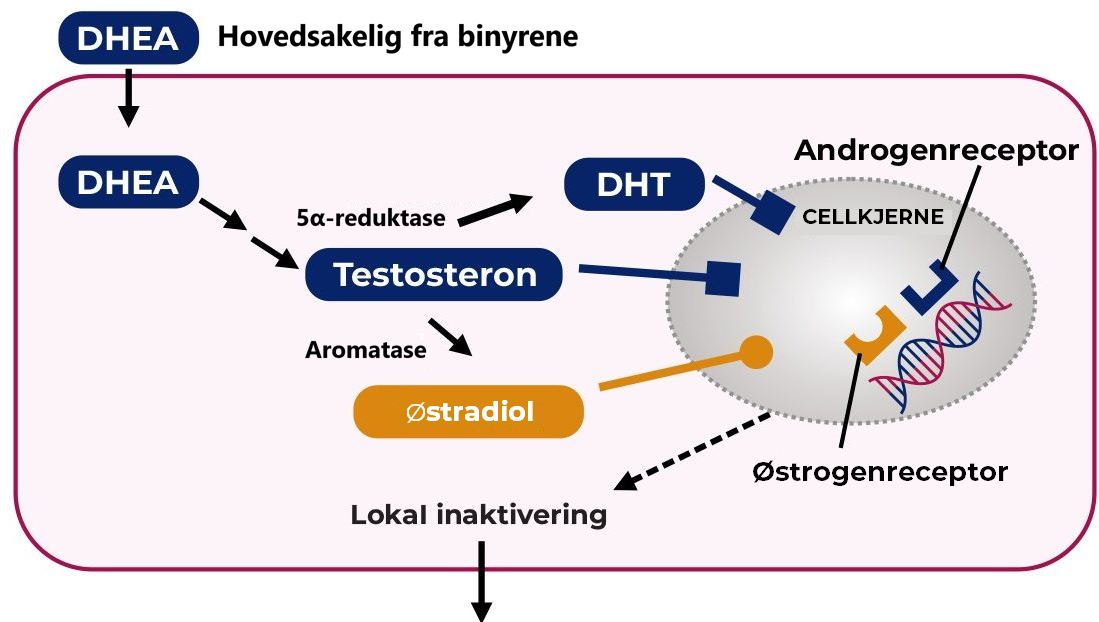
Illustrasjon tilpasset fra Boron, Medical Physiology 2005
Uendrede serumnivåer ved administrering av Intrarosa
Ved administrering av Intrarosa lå serumkonsentrasjonene av DHEA, testosteron og østradiol innenfor normalområdet for postmenopausale kvinner. (< 10 pg østradiol/ml [37 pmol/liter] og < 0,26 ng testosteron/ml)1
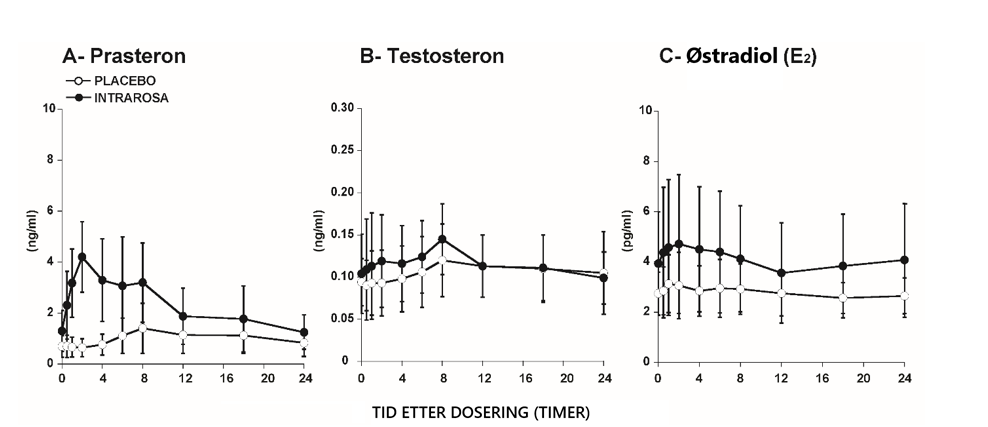
Serumkonsentrasjoner av DHEA (A), testosteron (B) og østradiol (C) målt over 24 timer på dag 7 efter daglig administrering av placebo eller Intrarosa (gjennomsnitt ± SD).
Diagrammene er tilpasset fra preparatomtalen (SPC) for Intrarosa.
Endometriesikkerhet
Sikkerhetsdata for Intrarosa er også hentet fra en ikke-komparativ, åpen sikkerhetsstudie med en varighet på ett år. Etter 52 ukers behandling med Intrarosa ble det ikke observert noen histologiske avvik i de 389 endometriebiopsiene som var evaluerbare ved studieslutt1.
Fysiologiske responser (objektive mål)
Effektdata ble hentet fra to dobbeltblinde, placebokontrollerte, pivotale fase III-multisenterstudier hos postmenopausale kvinner i alderen 40–80 år (gjennomsnittsalder 58,6 år i studie 1 og 59,5 år i studie 2) med vulvovaginal atrofi (VVA). Ved baseline hadde kvinnene ≤ 5,0 % overflateceller i vaginalutstryk, en vaginal pH på >5,0 og påvist dyspareuni (moderat til alvorlig) som det mest plagsomme symptomet på vulvovaginal atrofi.
Etter 12 ukers daglig behandling med en vagitorie som inneholdt prasteron 6,5 mg (n=81 i studie 1 og n=325 i studie 2), var endringen fra baselinesammenlignet med placebobehandling (n=77 i studie 1 og n=157 i studie 2) en signifikant forbedring av de tre koprimære endepunktene i begge studiene, nemlig
Symptomer (subjektive mål)
Dyspareuni/smerter ved samleie (koprimært endepunkt) ble rapportert som det mest plagsomme symptomet i effektstudiene med Intrarosa. Vurdering av dyspareuni ble utført ved baseline og etter 12 uker med gradering av alvorlighetsgrad.
Behandling med Intrarosa viste signifikant forbedring av dyspareuni sammenlignet med placebo (studie 1, p-verdi 0,0132; studie 2, p-verdi 0,0002).1
Anbefalt doseringen er én gang daglig, ved leggetid. Intrarosa vagitorier kan føres inn i vagina med applikatoren som følger med i pakningen, eller med fingeren.
Vagitorie (6,5 mg DHEA i hardfett), hvit til offwhite, avlang vagitorie med en lengde på cirka 28 mm og en diameter på cirka 9 mm i den bredeste enden. Pakning med 28 vagitorier i blister. 6 applikatorer følger med i pakningen.
Den hyppigst observerte bivirkningen var vaginal utflod. Dette skyldes hardfett, som fungerer som vehikkel i vagitoriene, smelter etter administrering. Samtidig skjer en forventet økning i mengden vaginalsekret som følge av behandlingen. Det er ikke nødvendig å avbryte behandlingen med Intrarosa på grunn av vaginal utflod. Bivirkninger som er observert med DHEA vagitorier 6,5 mg i kliniske studier, er oppført i tabellen nedenfor
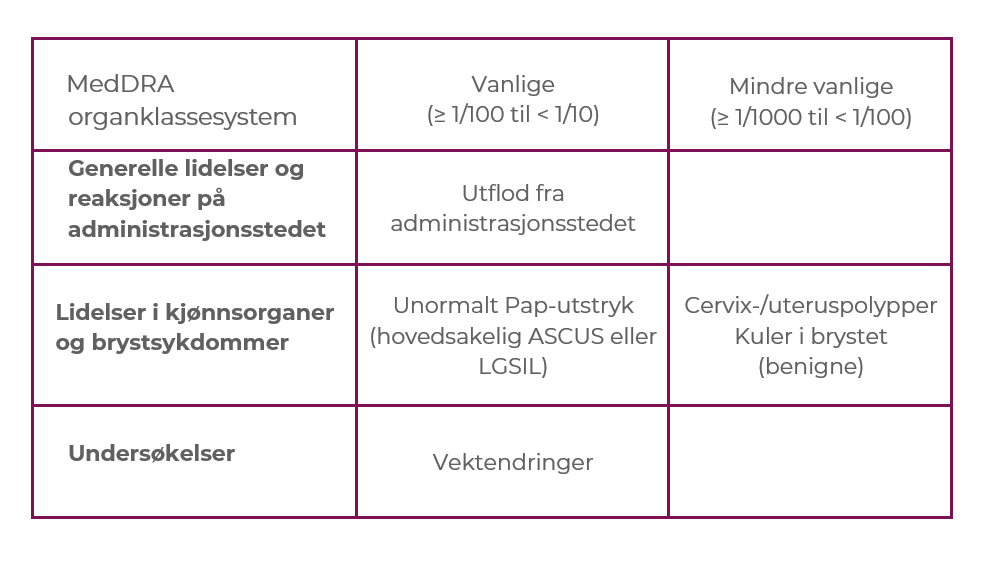
Se preparatomtale i (www.felleskatalogen.no) for fullstendig informasjon om bivirkninger.
Oppbevares ved høyst 30°C.
Skal ikke fryses.

INTRAROSA økte prosentandelen epitelceller med 7,71 prosentpoeng sammenlignet med placebo i studie 1 (P<0,0001) og 8,46 prosentpoeng sammenlignet med placebo i studie 2 (P<0,0001) (P<0.0001)13-15‡
†Gjennomsnittlig forandring fra Baseline i INTRAROSA -gruppen.
‡Forskjell sammenlignet med placebo=INTRAROSA (gjennomsnitt uke 12 – gjennomsnitt ved Baseline) – Placebo (gjennomsnitt uke 12 – gjennomsnitt ved Baseline).
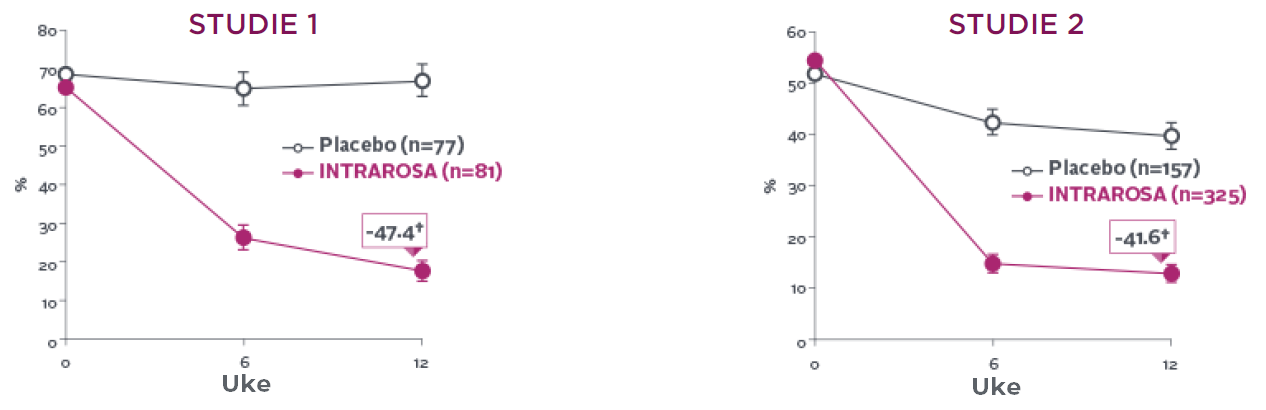 INTRAROSA reduserte prosentandelen av parabasale celler med 45,77 prosentpoeng sammenlignet med placebo i studie 1 (P<0,0001) og 29,53 prosentpoeng sammenlignet med placebo i studie 2 (P<0.0001)13-15‡
INTRAROSA reduserte prosentandelen av parabasale celler med 45,77 prosentpoeng sammenlignet med placebo i studie 1 (P<0,0001) og 29,53 prosentpoeng sammenlignet med placebo i studie 2 (P<0.0001)13-15‡
†Gjennomsnittlig forandring fra Baseline i INTRAROSA -gruppen.
‡Forskjell sammenlignet med placebo=INTRAROSA (gjennomsnitt uke 12 – gjennomsnitt ved Baseline) – Placebo (gjennomsnitt uke 12 – gjennomsnitt ved Baseline).
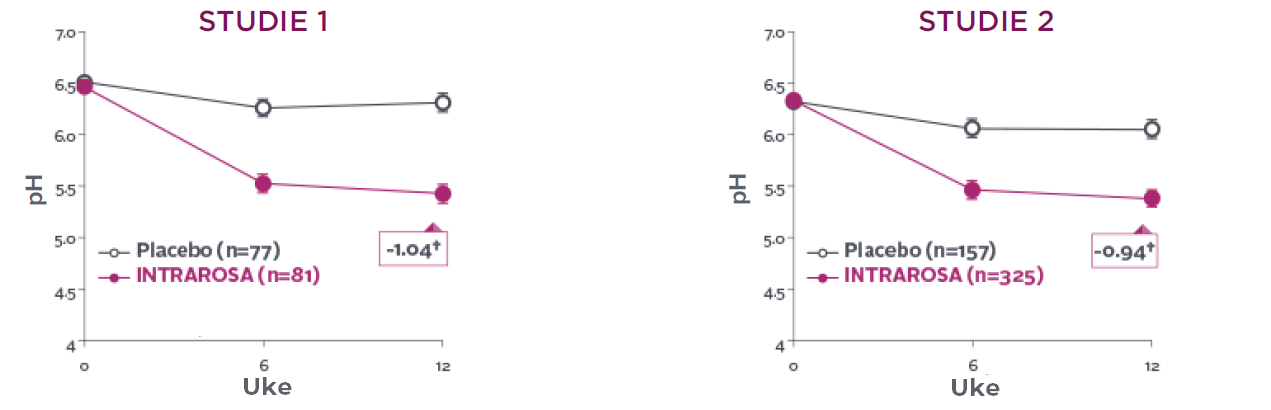 Intrarosa senket vaginalt pH med 0,83 prosentpoeng mer en placebo i studie 1 (P<0,0001) og 0,67 prosentpoeng mer en placebo i studie 2 (P<0,0001)
Intrarosa senket vaginalt pH med 0,83 prosentpoeng mer en placebo i studie 1 (P<0,0001) og 0,67 prosentpoeng mer en placebo i studie 2 (P<0,0001)
†Gjennomsnittlig forandring fra Baseline i INTRAROSA -gruppen.
‡Forskjell sammenlignet med placebo=INTRAROSA (gjennomsnitt uke 12 – gjennomsnitt ved Baseline) – Placebo (gjennomsnitt uke 12 – gjennomsnitt ved Baseline).

Endring i seksuell funksjon er et sekundært mål for effekt, er ikke en godkjent behandlingsindikasjon og er ikke evaluert av medisinske myndigheter. Tabellen viser forskjeller i FSFI mellom pasienter behandlet med Intrarosa eller
placebo (ERC-238) og endring fra baseline i den åpne langtidsstudien (ERC-230).
a p-verdi sammenlignet med placebo etter 12 uker. Studie ERC-238 (dobbeltblind, randomisert, placebokontrollert, 12 ukers behandling)b p-verdi sammenlignet med baseline etter 52 uker i ITT- populasjonen. Studie ERC-230 (open lable, 52 ukers behandling)c Resultatene tilsvarer forbedring av dysparenui symptom
 INTRAROSA ökade andelen ytliga celler med 4.71 procentenheter jämfört med placebo i Studie 1 (P<0.0001) och 8.46 procentenheter jämfört med placebo i Studie 2 (P<0.0001)13-15‡
INTRAROSA ökade andelen ytliga celler med 4.71 procentenheter jämfört med placebo i Studie 1 (P<0.0001) och 8.46 procentenheter jämfört med placebo i Studie 2 (P<0.0001)13-15‡
 INTRAROSA minskade andelen parabasalceller med 45.77 procentenheter jämfört med placebo i Studie 1 (P<0.0001) och 29.53 procentenheter jämfört med placebo i Studie 2 (P<0.0001)13-15‡
INTRAROSA minskade andelen parabasalceller med 45.77 procentenheter jämfört med placebo i Studie 1 (P<0.0001) och 29.53 procentenheter jämfört med placebo i Studie 2 (P<0.0001)13-15‡
 INTRAROSA minskade vaginalt pH med 0.83 enheter mer än placebo i Studie 1 (P<0.0001) och 0.67 enheter mer än placebo i Studie 2 (P<0.0001)13-15‡
INTRAROSA minskade vaginalt pH med 0.83 enheter mer än placebo i Studie 1 (P<0.0001) och 0.67 enheter mer än placebo i Studie 2 (P<0.0001)13-15‡
 Förändring av sexuell funktion är ett explorativt effektmått, är inte en godkänd behandlings-indikation och har inte värderats av medicinska myndigheter. Tabellen redovisar skillnader i FSFI mellan patienter som behandlats med Intrarosa eller placebo (ERC-238) respektive förändring från baseline i den öppna långtidsstudien (ERC-230).
Förändring av sexuell funktion är ett explorativt effektmått, är inte en godkänd behandlings-indikation och har inte värderats av medicinska myndigheter. Tabellen redovisar skillnader i FSFI mellan patienter som behandlats med Intrarosa eller placebo (ERC-238) respektive förändring från baseline i den öppna långtidsstudien (ERC-230).
a p-värde avser jämförelsen med placebo efter 12 veckor. Studie ERC-238 (dubbelblind, randomiserad, placebokontrollerad, 12 veckors behandling) Labrie, Derogatis et al. J Sex Med 2015;12:2401–2412
b p-värde avser jämförelsen med baseline efter 52 veckor i ITT-populationen. Studie ERC-230 (open label, 52 veckors behandling) Bouchard, Labrie et al. Horm Mol Biol Clin Invest 2016; 25(3): 181–19
c Resultaten motsvarar förbättring av dyspareunisymtom
13. Archer DF, Labrie F, Bouchard C, et al. Treatment of pain at sexual activity (dyspareunia) with intravaginal dehydroepiandrosterone (prasterone). Menopause, 22(9):950-963. 2015
14. Labrie F, Archer DF, Koltun W, et al. Efficacy of intravaginal dehydroepiandrosterone (DHEA) on moderate to severe dyspareunia and vaginal dryness, symptoms of vulvovaginal atrophy, and of the genitourinary syndrome of menopause. Menopause, 23(3):243-256. 2016
15. Intrarosa SPC December 2019
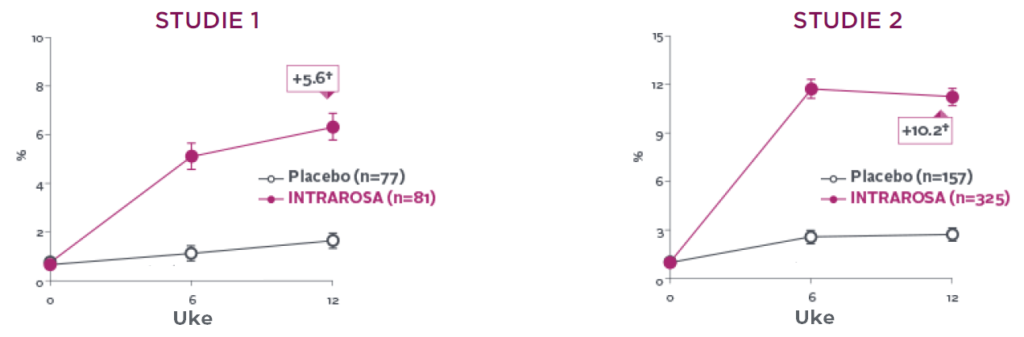
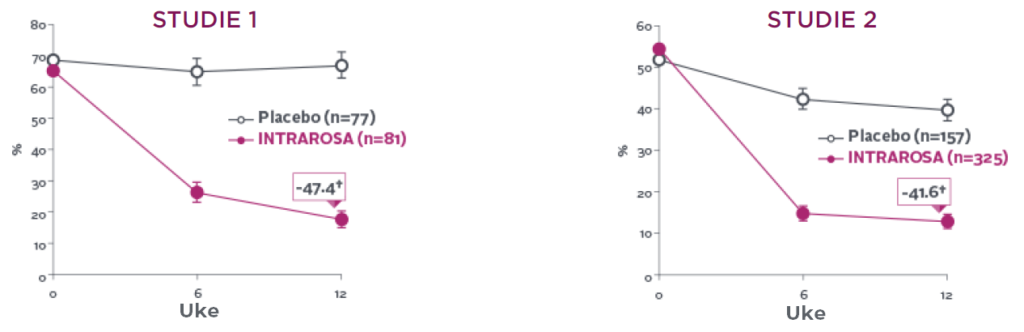
INTRAROSA reduserte prosentandelen av parabasale celler med 45,77 prosentpoeng sammenlignet med placebo i studie 1 (P<0,0001) og 29,53 prosentpoeng sammenlignet med placebo i studie 2 (P<0.0001)13-15‡

†Gjennomsnittlig forandring fra Baseline i INTRAROSA -gruppen.
‡Forskjell sammenlignet med placebo=INTRAROSA (gjennomsnitt uke 12 – gjennomsnitt ved Baseline) – Placebo (gjennomsnitt uke 12 – gjennomsnitt ved Baseline).
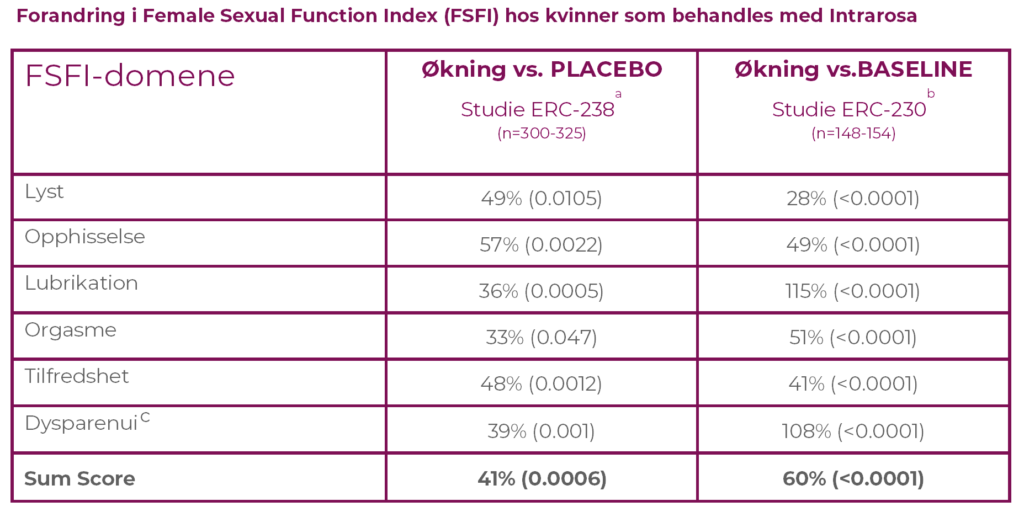
Endring i seksuell funksjon er et sekundært mål for effekt, er ikke en godkjent behandlingsindikasjon og er ikke evaluert av medisinske myndigheter. Tabellen viser forskjeller i FSFI mellom pasienter behandlet med Intrarosa eller placebo (ERC-238) og endring fra baseline i den åpne langtidsstudien (ERC-230).
a p-verdi sammenlignet med placebo etter 12 uker. Studie ERC-238 (dobbeltblind, randomisert, placebokontrollert, 12 ukers behandling) Labrie, Derogatis et al. J Sex Med 2015;12:2401–2412
b p-verdi sammenlignet med baseline etter 52 uker i ITT- populasjonen. Studie ERC-230 (open lable, 52 ukers behandling)
c Resultatene tilsvarer forbedring av dysparenui symptom
13. Archer DF, Labrie F, Bouchard C, et al. Treatment of pain at sexual activity (dyspareunia) with intravaginal dehydroepiandrosterone (prasterone). Menopause, 22(9):950-963. 2015
14. Labrie F, Archer DF, Koltun W, et al. Efficacy of intravaginal dehydroepiandrosterone (DHEA) on moderate to severe dyspareunia and vaginal dryness, symptoms of vulvovaginal atrophy, and of the genitourinary syndrome of menopause. Menopause, 23(3):243-256. 2016
15. Intrarosa SPC December 2019
Intrarosa er indisert for behandling av vulvovaginal atrofi hos postmenopausale kvinner med moderate til kraftige symptomer.
En gang per dag (ved leggetid, med eller uten applikator).
Oppbevares ved maks. 30°C.
Tåler ikke frost.
Vagitorie (6,5 mg DHEA I hardfett) hvitt til benhvitt, koniskt avsmalnende vagitorium. Lengde cirka 28 mm og diameter cirka 9 mm i den bredeste enden. 28 stk. Blister.
Bivirkninger som er observert med DHEA vagitorier 6,5 mg i kliniske studier, vises i tabellen nedefor:

1. Hvilken virkningsmekanisme kan forklare at pasienten rapporterer økt lyst ved lokal DHEA behandling?
2. Hvorfor trenger vi androgener ved behandling av vulvovaginal atrofi?
3. Hvordan påvirker androgen elastisitet og kontraktilitet i vagina?
4. Kan DHEA være mere effektivt enn bare østrogen for vulva og vestibulum?
6. Hva er grunnen til at enkelte kvinner som behandles med DHEA føler seg mere opplagt og sterkere?
7. Hva synes du om DHEA sammen med brystkreft behandling?
8. Hvorfor er det så stor forskjell på kontraindikasjonene for DHEA i Europa og USA?

Professor Andrea Genazzani
Universitetssykehuset i Pisa
Prof Genazzani er president for International Society of Gynecological Endocrinology og European Society of Gynecology.
Intrarosa är avsett för behandling av vulvovaginal atrofi hos postmenopausala kvinnor som har måttliga till svåra symtom.
Rekommenderad dos är 6,5 mg prasteron (ett vagitorium) en gang dagligen, vid sänggåendet. Produkten kan administreras med eller utan applikator.
Intrarosa förvaras i rumstemperatur (<30°C, får ej frysas).
▼ Detta läkemedel är nytt och därmed föremål för utökad övervakning. Intrarosa för behandling av postmenopausala symtom ska endast sättas in om symtomen har en negativ inverkan på livskvaliteten. Behandling med Intrarosa ska endast fortgå så länge nyttan överväger risken. För fullständig information vid förskrivning samt produktresumé (december 2019) se www.fass.se.
1. Intrarosa preparatomtale https://www.legemiddelsok.no/
2. Kim et al., J Menopausal Med. 2015 Aug; 21(2): 65–71.
3. Labrie F. et al, Menopause 18 30-43, 2011
4. Labrie et al, Climacteric. 16, 205-213, 2013